Därför är det viktigt att skydda processen för sterilitetstestning
Produktprover tas under hela produktionsprocessen och testas för mikrobiell kontaminering. I de flesta fall visar sterilitetstestet att produkten är fri från föroreningar, så att den kan skickas ut. När resultaten visar att en produkt är kontaminerad pausas utleveransen för att förhindra potentiella risker för patienterna.
Om din sterilitetsprocess inte är skyddad på ett lämpligt sätt kan kontaminering från miljön påverka testet och indikera att produkten är kontaminerad när den faktiskt inte är det. Detta kan leda till höga kostnader för tillverkaren och eventuell läkemedelsbrist för patienter, om batchen måste kasseras. Bidra till att skydda processen för sterilitetstestning från kontaminering i omgivningen, för att minska risken för falska positiva resultat.
Oavsett om ni använder membranfiltrering eller direkt inokulation kan en isolator erbjuda stora fördelar.

Upptäck vår isolator för sterilitetstestning
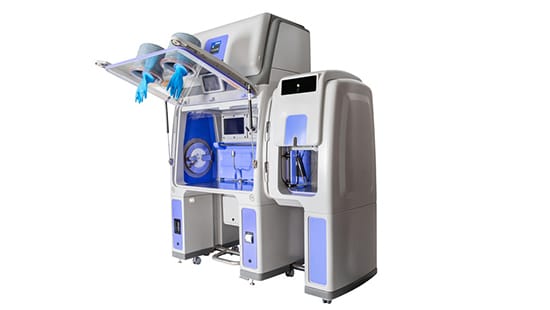
Ecolabs Bioquell Qube tillhandahåller en aseptisk miljö av klass A enligt ISO 5 och har integrerad Bioquell-teknik för väteperoxidånga*, vilket ger en validerad 6-logaritmisk avdödning av sporer på exponerade ytor på områdena där den används. Bioquell Cube har ett polymerhölje och kan integreras med Merck Millipore Symbio Flex-sterilitetspumpar, vilket gör den till en unik och idealisk lösning för sterilitetstestning.
* Vid användning i enlighet med anvisningarna på etiketten använder Ecolabs Bioquell-system Bioquell Hydrogen Peroxide Sterilant-AQ (EPA-registreringsnummer: 1677-277)
Är en isolator rätt val för dig? Har du rätt isolator?
Vad skulle ett falskt positivt resultat eller ett problem innebära för dig?
Att stoppa produktionen på grund av ett falskt positivt resultat kan leda till långa avbrott, onödig kassering av produkter, läkemedelsbrist och en sämre position för företaget på marknaden. Dessutom måste man ta hänsyn till extratiden, merarbetet och de ytterligare kostnaderna kopplade till CAPA-stegen.
Hur stor renrumsyta kräver processen?
Renrumsytan behöver ofta optimeras eftersom kostnaden per kvadratmeter för att bygga och driva utrymmet kan bli hög. En isolator som Bioquell Qube tar lite plats och kan till och med enkelt flyttas efter behov. Dessutom krävs ingen konstruktion och den kan användas i områden med lägre klassning. Kontakta Ecolab för specifikationer.
Kräver din process för sterilitetstestning ett renrum av klass B?
Med isolatorer kan du utföra testning i renrum med lägre klassning som kräver mindre eller ingen skyddsutrustning. Dessutom kan värdefullt renrumsutrymme reserveras för annan kritisk verksamhet, vilket kan bidra till att sänka driftkostnaderna eftersom renrum med högre klassning kräver en större ekonomisk investering och medför högre energi- och underhållskostnader.
Är din nuvarande process validerad och faktiskt upprepningsbar?
Automatiserad biologisk dekontaminering av inkommande material är en validerad process, vilket garanterar samma effektivitet för alla cykler. Detta bidrar till att ytterligare minska risken för falska positiva resultat.
Hur många sterilitetstest behöver du utföra under en dag?
Renrumsytan behöver ofta optimeras eftersom kostnaden per kvadratmeter för att bygga och driva utrymmet kan bli hög. En isolator som Bioquell Qube tar lite plats och kan till och med enkelt flyttas efter behov. Dessutom krävs ingen konstruktion och den kan användas i områden med lägre klassning. Bioquell Qube kan till exempel hantera upp till 60 test per dag, beroende på konfigurationen. Kontakta Ecolab för specifikationer.
Outsourcar du processen för sterilitetstestning?
Det finns fördelar med att utföra processen internt, däribland större kontroll över processen, kostnadsbesparingar på lång sikt och snabbare resultat. Med en isolator som kan placeras i CNC-områden eller renrum av lägre klass kan detta bli verklighet för företag, trots förhandskostnaderna relaterade till utrustningen.

Effekten av underkända test
Ett underkänt test kan få allvarliga konsekvenser för en läkemedelstillverkare eftersom det normalt leder till
- att produktbatchen som inte fick godkänt inte kan släppas och kan behöva kasseras
- ytterligare rengöring och desinficering av tillverkningsutrymmen
- att tillsynsmyndigheter blir inblandade
- ekonomisk förlust för tillverkaren
- tidskrävande utredningar
- läkemedelsbrist för patienter
- att tillverkningen av ytterligare produkter stoppas medan utredningarna genomförs
Men underkända sterilitetstest innebär inte alltid att produkten är kontaminerad.
Ett falskt positivt resultat kan uppstå när kontaminering från omgivningen eller användaren som utför testet lyckas ta sig in i själva testet, vilket gör att det underkänns. En produkt klassas som kontaminerad trots den faktiskt är fri från skadliga mikroorganismer.
När ett sterilitetstest underkänns är det tillverkaren som ansvarar för att bevisa att det underkända resultatet har uppstått på grund av kontaminering från användaren och/eller labbmiljön, vilket kan vara svårt. Därmed leder falska positiva resultat ofta till att verksamma produkter som uppfyller alla krav kasseras i onödan.
Skydda verksamheten med en isolator för sterilitetstestning

Regelverk för isolatorer:
- I EU:s principer och riktlinjer för god tillverkningssed, bilaga 1, avsnitt 10.6 fastställs att
”sterilitetstestning ska utföras under aseptiska förhållanden”
- FDA:s vägledning för branschen angående sterila läkemedel tillverkade med aseptiska processer tar detta ett steg längre och fastställer i avsnitt XI att
”användningen av isolatorer för sterilitetstestning minimerar risken för falskt positiva testresultat”
- Enligt EU:s principer och riktlinjer för god tillverkningssed, bilaga 1, är en isolator
”en försluten enhet som kan utsättas för reproducerbar invändig biologisk dekontaminering med en intern arbetszon som uppfyller kraven på grad A och erbjuder kontinuerlig isolering av det invändiga utrymmet från den yttre miljön utan några kompromisser”

Isolatorer har flera funktioner för att skyddaaseptiska processer, bland annat
- lufttäta/uppblåsbara tätningar på alla luckor
- spärrar som förhindrar att luckorna öppnas när aseptiska förhållanden har uppnåtts (efter biologisk dekontaminering)
- enkelriktade luftflöden på 0,36–0,45 m/s (för att följa riktvärdena i EU:s principer och riktlinjer för god tillverkningssed, bilaga 1)
- HEPA-filter för rengöring av inkommande luft
- tryckinställningar, separat trycktestning av inneslutna utrymmen och handskar
- miljöövervakningssystem för att bekräfta att miljön förblir aseptisk under användning
- larm för luftflöde och tryck
- biologiska dekontamineringssystem med väteperoxidånga som uppnår 6-logaritmisk spordödande effekt* för att eliminera kontaminering på de inneslutna ytorna och inkommande material som behövs för testprocessen
* Vid användning i enlighet med anvisningarna på etiketten använder Ecolabs Bioquell-system Bioquell Hydrogen Peroxide Sterilant-AQ (EPA-registreringsnummer: 1677-277)
Fördelar med isolatorer
Isolatorer minskar främst risken för falska positiva resultat av sterilitetstestning, vilket kan spara tillverkare av sterila produkter miljoner genom att minimera onödig kassering av produkter.
En sekundär fördel är att isolatorer även kan ge stora besparingar av driftskostnader.
Till skillnad från biologiska säkerhetsskåp (BSC)/laminärt luftflöde, som måste finnas i ett renrum av klass B, kan isolatorer placeras i ett lägre klassat renrum av klass C/D. Detta kan leda till stora besparingar till följd av:
- energikostnaden för ventileringssystem med lägre kapacitet
- lägre personalkostnader (för rengöring och desinficering)
- mindre underhåll av renrummen
- lägre kostnader för förbrukningsvaror kopplade till rengöring och desinficering
- mindre krav på skyddsutrustning
- större effektivitet för operatörer eftersom mindre användning av skyddsutrustning innebär att de kan arbeta under längre perioder
1Kostnad för ett renrum per kvadratfot, renrumsteknik, 28 februari 2018


Jämförelse mellan traditionella isolatorer i rostfritt stål och Bioquell Qube